L'HÉMORRAGIE
DEFINITION
Perte de sang en dehors du compartiment vasculaire.
Elle peut être due à :
-
Une atteinte de l’intégrité des vaisseaux : soit par rupture totale de la paroi soit par atteinte de l’endothélium.
-
Une atteinte de l’hémostase (« coagulation ») : soit par atteinte des plaquettes (par diminution du nombre de plaquettes (thrombopénie) ou atteinte de leur fonction (thrombopathie)) soit par atteinte des facteurs de coagulation.
Les processus de la coagulation

Lors d’une atteinte vasculaire, une effraction de l’endothélium peut entrainer la fuite de sang en dehors du vaisseau (hémorragie). Des mécanismes vont alors se mettre en place pour limiter cette perte : c’est le phénomène d’hémostase. Celui-ci se décompose en plusieurs étapes.
-
Vasoconstriction : précoce, elle limite l’arrivée de sang au niveau du territoire vasculaire lésé.
-
Hémostase primaire : c’est la phase plaquettaire. La brèche vasculaire expose une partie de tissu conjonctif périvasculaire sur lequel vont venir adhérer les plaquettes. Ces dernières vont ensuite libérer des molécules qui vont attirer et recruter d’autres plaquettes qui vont venir s’agréger elles aussi. Il y a formation du « clou plaquettaire ».
-
Hémostase secondaire : elle fait intervenir les facteurs de coagulations. Ces derniers sont essentiellement synthétisés dans le foie sous l’action de la vitamine K sauf le facteur tissulaire (TF, facteur III) qui lui est présent dans les tissus en dehors du compartiment vasculaire ou sur la membrane de cellules inflammatoires. Un ensemble de réaction aboutit à l’activation de la thrombine (facteur II activé) qui va fractionner le fibrinogène soluble en plusieurs molécules de fibrine insolubles. Cette fibrine va ensuite consolider le clou plaquettaire et former un thrombus (plaquettes + fibrine + hématies/neutrophiles).
-
Régulation : des mécanismes de régulation existent en particulier pour freiner ce phénomène de coagulation et éviter l’extension et la croissance du thrombus. Les principaux sont : le TFPI qui inhibe le facteur tissulaire, le complexe « protéine C - protéine S - thrombomoduline » qui inhibe des réactions dans la voie d’activation de la thrombine, et l’antithrombine qui inhibe principalement la thrombine.
-
Fibrinolyse : cette étape se met rapidement en place pour éviter que le thrombus formé ne persiste. Plusieurs facteurs sont responsables de l’activation de l’enzyme clé de cette étape : la plasmine. Celle-ci à pour rôle de lyser la fibrine pour affaiblir le clou plaquettaire. Les résidus obtenus sont appelés produits de dégradation de la fibrine (PDF). Des mécanismes de régulation existent aussi pour cette voie.
PATHOGENIE & ETIOLOGIE
Atteinte de l’intégrité des vaisseaux :
-
On distingue tout d’abord des processus capables de rompre totalement des vaisseaux.
-
C’est le cas lors de traumatismes mais également lors de processus inflammatoires ou néoplasiques invasifs.
-
Certains agents infectieux, notamment fongiques peuvent également être à l’origine d’hémorragie (exemple: hémorragie rétinienne en cas de cryptococcose systémique, aspergillose).
-
-
D’autres mécanismes favorisent simplement une atteinte locale des endothéliums permettant une diapédèse des hématies.
-
Cela englobe des processus infectieux comme lors d’endotoxémies ou certaines atteintes virales (adénovirus canin de type 1 par exemple) ou parasitaires (exemple : dirofilariose, angiostrongylose…).
-
Des agents chimiques peuvent également endommager l’endothélium comme l’urée lors de syndrome urémique causé par une insuffisance rénale sévère.
-
Des dépôts d’immuns complexes peuvent être à l’origine de vascularite (exemple : hypersensibilité de type III, Péritonite Infectieuse Féline).
-
Enfin des troubles des flux sanguins (infarcissement, stase, infarctus…) peuvent provoquer des atteintes endothéliales en provoquant leur nécrose par hypoxie.
-
Atteinte plaquettaire :
On distingue soit un déficit en plaquette (thrombopénie) soit une atteinte de leur fonction (thrombopathie). En ce qui concerne la thrombopénie, on compte quatre grandes causes :
-
Défaut de production : il s’agit d’une atteinte des précurseurs plaquettaires dans la moelle. Il peut s’agir d’atteinte infectieuse(principalement virale), d’agents cytotoxiques (radiation, médicaments etc) ou de tumeurs envahissant la moelle empêchant une synthèse correcte.
Exemple: parvovirus canin et félin, leucémie etc.
-
Destruction en excès : souvent le résultat de maladies à médiation immune. Il peut s’agir de maladies auto-immunes dirigées contre les plaquettes (exemple : lupus érythémateux disséminé) ou bien de maladies qui vont altérer la membrane des plaquettes qui seront alors détruites.
-
Surconsommation : c’est le résultat d’une atteinte endothéliale diffuse ou d’une activation plaquettaire trop intense à l’origine d’une coagulation intravasculaire disséminée (CIVD).
-
Séquestration : une thrombopénie peut apparaître en cas de séquestration des plaquettes dans la rate.
Les thrombopathies entrainent principalement d’un défaut d’agrégation plaquettaire. Cela est retrouvé dans certains syndromes qui sont très rares. Une urémie importante peut également être à l’origine d’une thrombopathie ou l’utilisation de certains AINS (comme l’aspirine).
Pathogénie de la coagulation intravasculaire disséminée (CIVD)
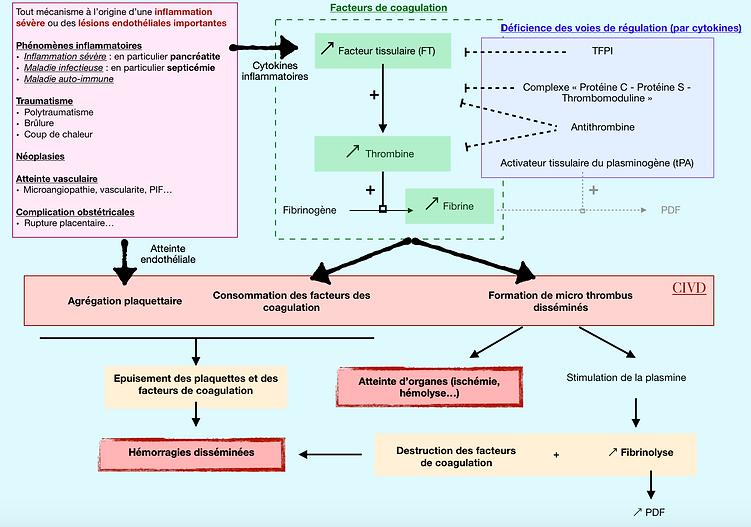
La Coagulation Intravasculaire Disséminée (CIVD) est un syndrome qui se met en place à la suite d’une atteinte pathologique sous-jacente. Le plus souvent il s'agit d’une inflammation sévère comme lors de pancréatite ou de polytraumatismes, ou de lésions endothéliales importantes comme lors de septicémies.
Phase d’hypercoagulabilité :
-
Ces affections provoquent une hausse du facteur tissulaire soit parce qu’il est plus exposé à cause de nombreuses brèches vasculaires, soit parce qu’il est amplifié par des molécules inflammatoires (cytokines) et/ou des cellules inflammatoires. Une élévation de ce facteur va être à l’origine d’une stimulation de l’hémostase secondaire (facteurs de coagulation) aboutissant à une élévation de la concentration en thrombine et par conséquent celle de la fibrine.
-
Parallèlement, les cytokines inflammatoires ont tendance à inhiber les voies de freinage de cette hémostase secondaire, ainsi qu’inhiber les facteurs favorisant la fibrinolyse. Cela va amplifier d’avantage la formation de fibrine.
-
Des agrégations plaquettaires ont également lieu en parallèle au niveau des lésions endothéliales.
L’ensemble de ces phénomènes est à l’origine de la CIVD.
Conséquences :
-
La formation importante de fibrine est à l’origine de micro-thrombus disséminés qui peuvent provoquer de multiples ischémies voire des infarcti et altérer de nombreux organes.
-
Les agrégations plaquettaires et la forte stimulation de l’hémostase secondaire provoquent un appauvrissement en plaquettes et facteurs de la coagulation.
-
La hausse en concentration de fibrine entraine quand même à terme une stimulation de la fibrinolyse par stimulation importante de la plasmine. Celle-ci dégrade la fibrine en PDF mais aussi les facteurs de la coagulation lorsqu’elle est stimulée en excès. Cela amplifie l’appauvrissement en ces facteurs.
Ainsi, on obtient finalement une phase d’hypocoagulabilité par thrombopénie, déficit en facteurs de la coagulation mais aussi du fait des fortes concentrations en plasmine qui limiteraient dans tous les cas la formation de fibrine pour consolider des clous plaquettaires. Il en résulte la formation de nombreuses hémorragies disséminées.
Atteinte des facteurs de coagulation :
-
Défaut de production de facteurs fonctionnels :
-
soit un manque de production lors d’insuffisance hépatique (le foie étant l’organe responsable de leur synthèse),
-
soit par un défaut de production de facteurs fonctionnels comme lors d’un déficit en vitamine K, hormone impliquée dans leur activation fonctionnelle.
-
Une synthèse primaire de facteurs anormaux est très rare et principalement d’origine génétique.
Exemple: intoxication aux anti-vitamines K de certains rodenticides, hépatite chronique etc.
-
-
Surconsommation : comme pour les plaquettes, un excès de consommation est retrouvé lors de coagulation intravasculaire disséminée (CIVD).
Schéma étiologique récapitulatif de l'hémorragie

ASPECT MACROSCOPIQUE
Nomenclature des lésions hémorragiques

Une CIVD pourra être reconnue lors de la présence de nombreuses micro-hémorragies (pétéchies) disséminées.
-
Couleur : rouge sombre
-
Taille/Forme : variable
-
Localisation : tissulaire, cavitaire ou extériorisée
Le sang peut être retrouvé sous forme coagulée ou non

On observe la présence de petite plages hémorragiques punctiformes multifocales à la surface des organes (1,2,3). Il s’agit de pétéchies. Sur les autres photos (4,5,6), les plages hémorragiques sont plus étendues, et l’on parle de suffusions. EnvA; https://noahsarkive.cldavis.org, photos F02443-F02075-F20187-F03936-F33182.

On observe la présence de sang associé à des parasites dans ce contexte d’entérite hémorragique (1). Les photos (3,4) montrent la présence d’une collection de sang au sein d’une cavité néoformée sphérique bien délimitée (tête de flèche) : il s’agit d’hématomes spléniques. Enfin, une collection de sang peut se produire au sein d’une cavité pré-existante, comme un hémothorax (2). Zachary, 2017 ; https://noahsarkive.cldavis.org, photos F33003-F33379-F05476.
ASPECT MICROSCOPIQUE
Une hémorragie est identifiée par la présence d’hématie en dehors du compartiment vasculaire dans le milieu interstitiel. Lors d’hémorragie importante, si une grande quantité d’hématies envahit le tissu, une nécrose peut se mettre en place accompagnée d’une réaction inflammatoire. De la fibrine (aspect fibrillaire hyalin, rose en coloration standard) peut également être retrouvée.
Un hématome ancien est reconnaissable par une collection d’hématies dans une structure capsulaire fibreuse.
Une chronicité peut être identifiée grâce aux sidérophages, qui sont des macrophages chargés en hémosidérine (cytoplasme brun), témoins d’une résorption progressive de l’hémorragie.

Hématome (rate, chat) : on observe un hématome, c’est à dire une collection de sang dans un cavité néoformée (pointillés), qui déforme la paroi splénique. EnvA
Hémorragie (glande salivaire, chien) : de multiples hématies sont retrouvées en dehors du compartiment vasculaire (*) à l’origine d'une hémorragie plutôt diffuse. On note également une congestion passive des veines et des capillaires (tête de flèche). EnvA

Hémorragie (poumon, chien) : des hématies sont observées dans les alvéoles pulmonaires ainsi que du plasma (*) éosinophile, traduisant sa richesse en protéines. Des macrophages alvéolaires sont présents pour nettoyer la zone (tête de flèche) ainsi que des granulocytes neutrophiles (flèche), témoin d’une inflammation en cours. EnvA
Micro-hémorragies (encéphale, chien, x10) : on observe de petites hémorragies multifocales (têtes de flèche). Macroscopiquement, cela se traduirait par des pétéchies. https://noahsarkive.cldavis.org, photo F04148
L’Essentiel
-
Une hémorragie est une perte de sang en dehors du compartiment vasculaire.
-
C’est une lésion peu spécifique car retrouvée dans de nombreux cas.
-
Trois grandes causes possibles : atteinte vasculaire, atteinte des plaquettes ou atteinte des facteurs de coagulation.
-
En cas de nombreuses lésions hémorragiques de petite taille (pétéchies), penser à la coagulation intravasculaire disséminée (CIVD) et penser à une cause pathologique sous-jacente.